
近日,浙大二院眼科中心、浙江大学眼科医院姚克教授团队在生物医学工程领域权威期刊《Bioengineering & Translational Medicine》(影响因子10.711)发表题为“Ferrostatin-1-loaded liposome for treatment of corneal alkaliburn via targeting ferroptosis”的研究论文。

该研究首次发现了角膜碱烧伤过程中存在铁死亡这一新型细胞死亡方式,并于国际上率先利用脂质体递送铁死亡特异性抑制剂Ferrostatin-1(Fer-1),有效改善碱烧伤导致的角膜损伤,并缓解碱烧伤引起的炎症反应和新生血管形成。负载Fer-1的脂质体相比于游离Fer-1具有更显著的治疗效果,且安全性良好,有望成为应用于临床靶向铁死亡、改善碱烧伤角膜的潜在新型治疗方式。
角膜碱烧伤作为眼科急诊中常见的疾病之一,常引起角膜混浊和新生血管形成,严重时甚至可导致患者丧失视力。现有疗法存在有创、疗效有限及药物副作用等不足。因此,探索针对角膜碱烧伤更安全、有效、便捷的新疗法成为近年来眼科研究的热点。
受限于复杂的生理学和解剖学结构,眼部药物递送一直是重大的技术挑战。脂质体是由磷脂和胆固醇组成的微型囊泡,疏水性药物和亲水性药物可以分别封装在其磷脂双分子层和水核内。脂质体具有良好的角膜穿透性和生物相容性,可以实现药物的持续递送。因此,脂质体可作为潜在的纳米载体用于眼部药物递送以修复受损角膜。本研究旨在探索角膜碱烧伤发生发展过程中的新机制,进一步针对其靶点利用脂质体递送治疗药物,从而实现精准、安全、有效、便捷的治疗目的。
前期研究提示,碱烧伤会引起活性氧自由基(ROS)增多,后者通过激活炎症反应、促进角膜新生血管生长等对角膜造成严重损伤。此外,新生血管还易导致角膜发生脂质渗出和沉积。铁死亡是一种脂质过氧化产物及铁离子依赖的程序性细胞死亡方式。无论是ROS还是游离铁离子增多,均可引发脂质过氧化产物堆积,从而攻击细胞膜和线粒体、引发铁死亡。多项研究提示铁死亡特异性抑制剂Fer-1可改善多种铁死亡相关疾病的发生发展,表明其用于临床转化治疗相关疾病的潜力。然而,铁死亡在角膜碱烧伤中的作用及Fer-1的疗效尚不清楚。
本研究发现,与健康对照相比,碱烧伤后的小鼠眼表出现明显的角膜混浊、新生血管生长,且组织学结果显示出明显的角膜水肿、炎性细胞和新生血管浸润。Fer-1给药可显著改善这些损伤,提示碱烧伤引起的角膜损伤中存在铁死亡。
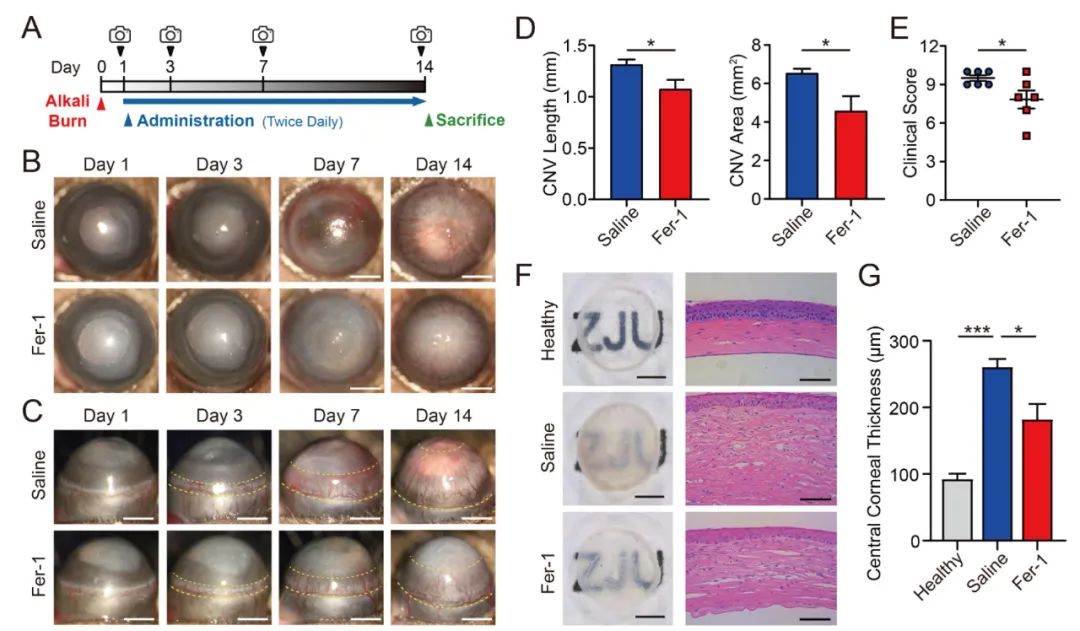
Fer-1给药改善碱烧伤引起的小鼠角膜损伤
后续实验表明,碱烧伤导致铁死亡促进通路被激活而阻碍通路被抑制,同时大量ROS攻击线粒体,二者共同促进了角膜组织铁死亡的发生。Fer-1处理改善了上述指标的异常表达,提示铁死亡可作为治疗角膜碱烧伤的靶点。
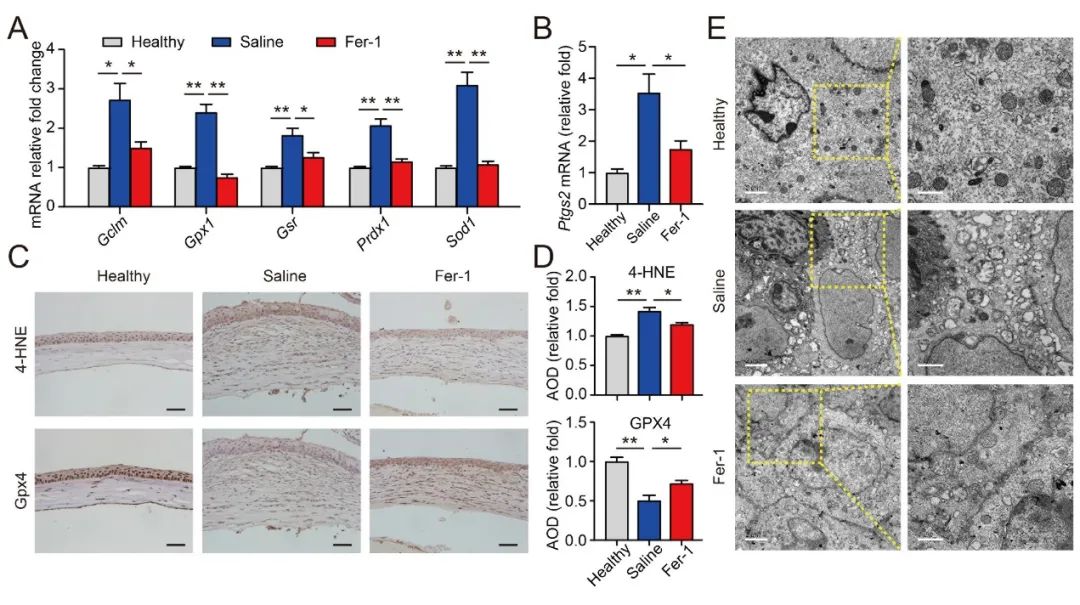
小鼠角膜碱烧伤损伤过程中存在铁死亡
滴眼给药具有简单、安全等优势,但受限于泪液冲刷、眨眼反射及眼表屏障的存在,传统滴眼液的生物利用度往往很低。此外,由于Fer-1水溶性差且在体内有效作用时间较短,其在临床治疗中的应用具有一定的局限。虽然一些赋形剂材料可用作增溶剂来递送药物,但对眼部的刺激性和组分的复杂性限制了其临床应用。相比之下,脂质体由于制备工艺简单成熟,可用于大规模量产。其生物相容性也得到了广泛认可,自1995年的阿霉素脂质体以来,已有大量的脂质体药物被 FDA 批准用于临床。因此,脂质体负载技术更有可能影响临床实践并推动医疗产品革新。基于此,本研究团队进一步通过薄膜分散法制备了负载Fer-1的脂质体滴眼液。多项材料学表征显示,与游离药物相比,脂质体负载的药物表现出了优异的药物缓释行为、并有效提高了细胞摄取及眼表停留时间,表明脂质体递送系统有助于提高药物的生物利用度。
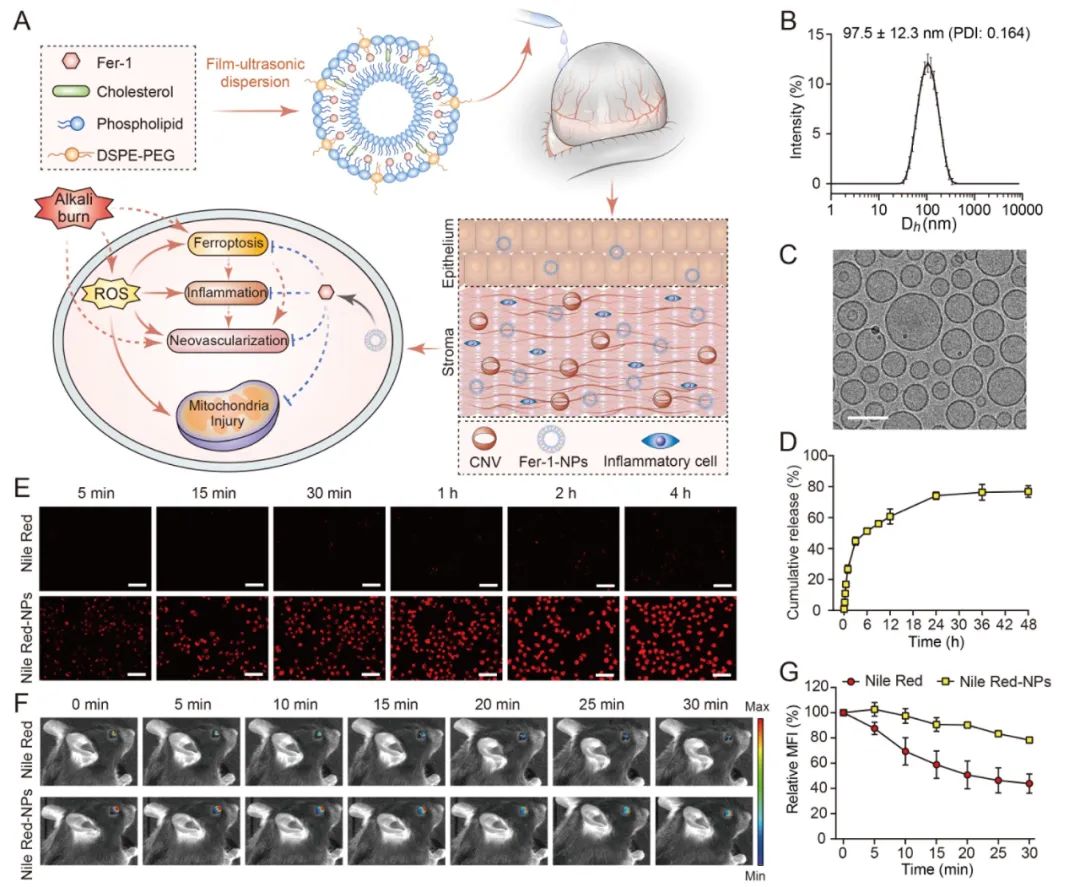
Fer-1脂质体可提高药物的生物利用度
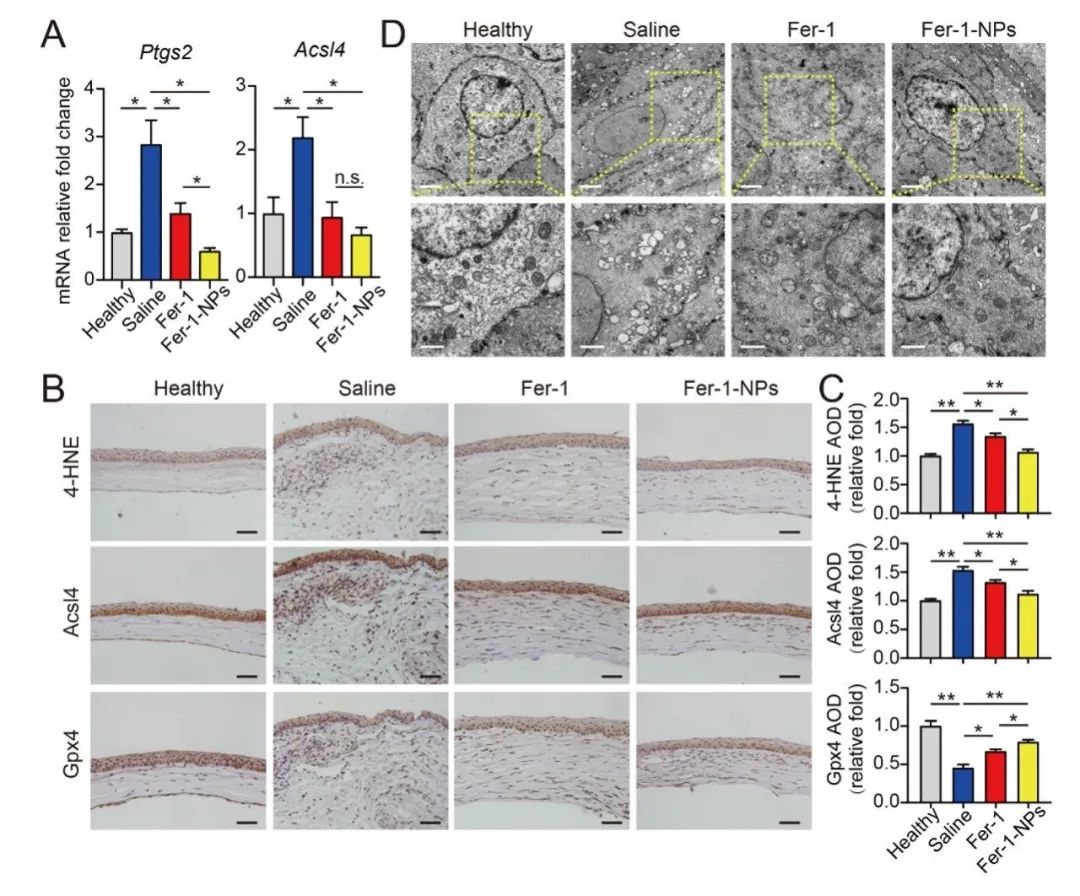
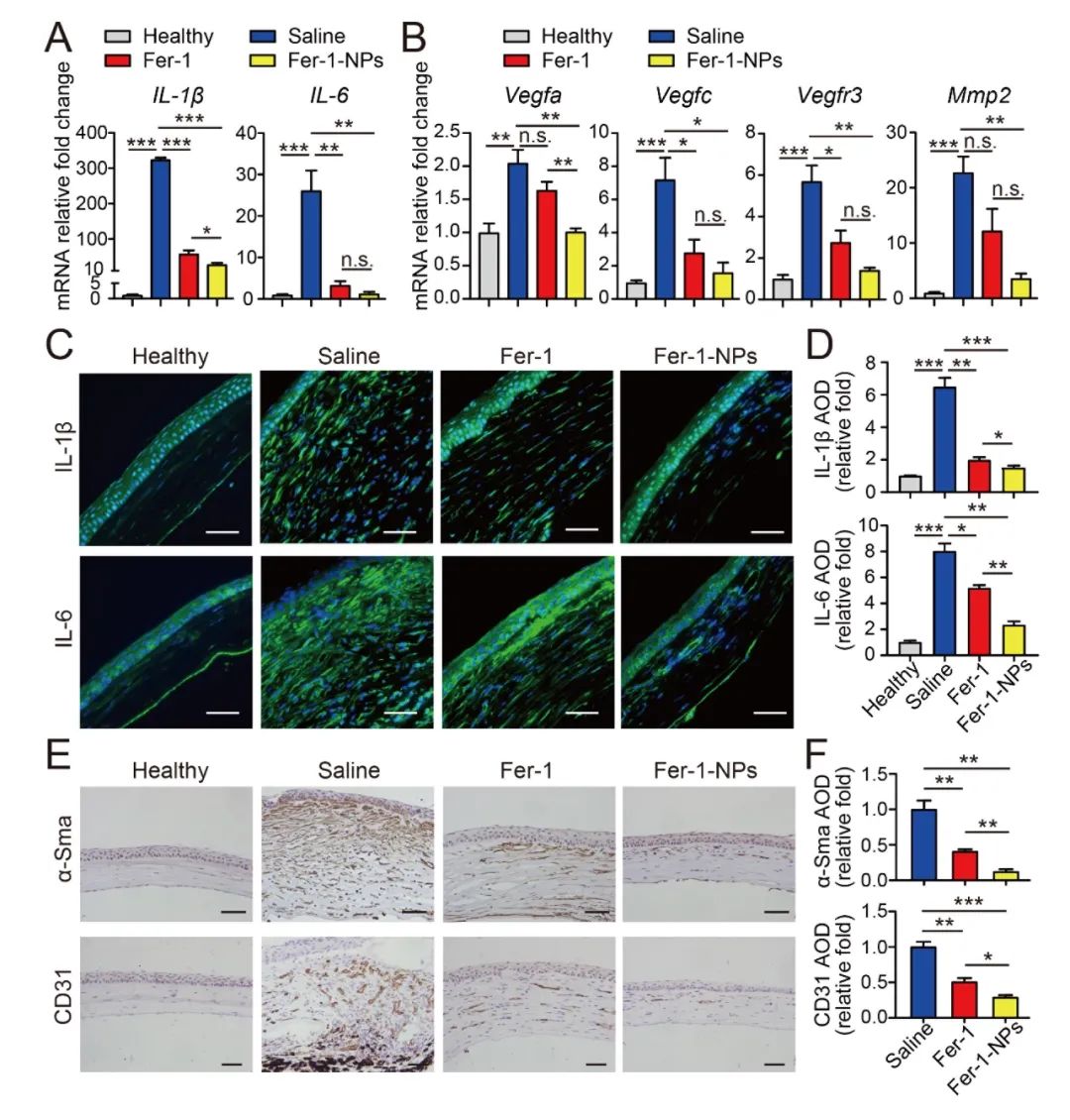
进一步的治疗效果及作用机制研究表明,在Fer-1脂质体处理组中,除了铁死亡相关指标,碱烧伤诱导的角膜损伤、炎症反应及新生血管形成均得到有效改善,且疗效显著优于游离Fer-1组。包括炎症指标IL-1β和IL-6,新生血管相关调控因子Vegfa,Vegfc,Vegfr3,Mmp2,α-Sma及CD31的异常表达均可被游离Fer-1及Fer-1脂质体所挽救,且Fer-1脂质体的作用更明显。以上结果表明,Fer-1脂质体对角膜碱烧伤损伤的治疗作用显著优于游离Fer-1。另外,本研究评估了Fer-1脂质体的安全性,体内外的实验结果均表明Fer-1脂质体无明显毒副作用。
浙江大学眼科医院、浙二眼科中心姚克教授,韩海杰研究员为本文通讯作者,浙江大学医学院博士后王凯、蒋丽和钟乐扬为论文共同第一作者。研究工作得到了国家自然科学基金、国家重点研发项目、浙江省重点研发项目以及浙江省自然科学基金等资助。
原文链接:https://doi.org/10.1002/btm2.10276

通讯作者:姚克 教授
主任医师,博士生导师
浙江大学眼科医院院长、浙江大学眼科研究所所长、浙江大学医学院附属第二医院眼科中心主任。国际眼科科学院院士、浙江省特级专家。中华医学会眼科学分会主任委员,亚太白内障及屈光手术学会候任主席,国际眼科理事会常务理事,亚太眼科学会中国区负责人,亚太眼科学院理事,国际人工晶状体植入俱乐部会士,中华医学会常务理事,中国医师协会常务理事,中华眼科杂志主编,中华医学会眼科学分会白内障及屈光手术学组组长,浙江省科协主席,浙江省医学会会长。以第一获奖人获3项国家科技进步二等奖、3项浙江省科技进步一等奖、10余项省科技重大贡献奖等省部级奖和瑞士眼科Alfred-Vogt奖、国际眼科理事会Mark Tso金苹果奖、亚太白内障及屈光手术学会金奖、意大利眼科学会Antonio Scarpa奖、国际讲座奖等。发表学术论文473篇,其中SCI收录258篇,获7项国家发明专利,并先后获得国家自然科学基金重点项目、“十一五”及“十二五”国家支撑项目和国家基金重点和面上项目等国家及省部级重大项目30余项。

通讯作者:韩海杰
特聘研究员,博士生导师
2018年博士毕业于浙江大学高分子科学与工程学系,并于同年加入浙江大学医学院附属第二医院眼科中心工作。主要研究领域为高分子纳米药物载体的设计及其在眼科领域的应用。以第一/通讯作者在Journal of the American Chemical Society, ACS Nano, Small, Bioactive Materials, Bioengineering & Translational Medicine等学术期刊上发表论文15篇,3篇论文入选ESI高被引论文,作为负责人主持承担了包括国自然青年基金、浙江省青年基金、浙江省联合基金等多项国家及省部级项目。

第一作者:王凯 博士
2021年博士毕业于浙江大学临床医学八年制专业,师从姚克教授,目前在浙江大学医学院从事临床医学博士后研究工作。主要研究方向为纳米药物及生物材料在眼病诊疗中的应用,利用孟德尔随机化探究眼病机制。以第一/共同作者在Bioengineering & Translational Medicine, Journal of Clinical Endocrinology & Metabolism, Blood, BMC Medicine等学术期刊上发表论文16篇,参与多项国家基金项目。