

浙江大学医学院附属第二医院眼科中心/浙江大学眼科医院姚克/韩海杰团队面向重要致盲眼病,开展眼用生物材料的基础和转化研究。该团队最近在ACS Nano(IF15.8) ,Science Advances(IF11.7)和Advanced Science(IF14.3)发表了三篇原创研究成果,探索眼病防治新策略。

1
浙江大学眼科医院/浙大二院眼科中心姚克教授和韩海杰研究员团队提出了基于“以药递药”策略,设计并制备了一种星型抗菌肽聚合物(SAPP)负载群体感应抑制剂槲皮素(QCT)的复合物,QCT@SAPP(图1)。由星型抗菌肽聚合物(SAPP)作为载体,通过其特殊的结构和正电荷特性,能够有效渗透到致密的细菌生物被膜中,破坏细菌膜,杀灭细菌。SAPP不仅作为抗菌成分,同时也是QCT的载体,实现QCT的持续释放。QCT@SAPP不仅能够显著抑制生物被膜的群体感应并破坏细菌生物被膜,提升抗菌效果,而且具有抗炎抗氧化的效果,加速角膜炎的恢复。研究表明,QCT@SAPP在小鼠模型中成功治疗了细菌性角膜炎,并且无明显毒性,表现出优异的治疗效果。该研究以“Drug in Drug: Quorum Sensing Inhibitor in Star-shaped Antibacterial Polypeptides for Inhibiting and Eradicating Corneal Bacterial Biofilms”为题发表在《ACS Nano》上(ACS Nano, 2025, 19(2): 2268–2285)。文章第一作者是浙江大学博士研究生卢周煜、浙大二院/浙大眼科医院范文捷医生和叶洋医生。该研究得到国家自然科学基金和浙江省自然科学基金的支持。
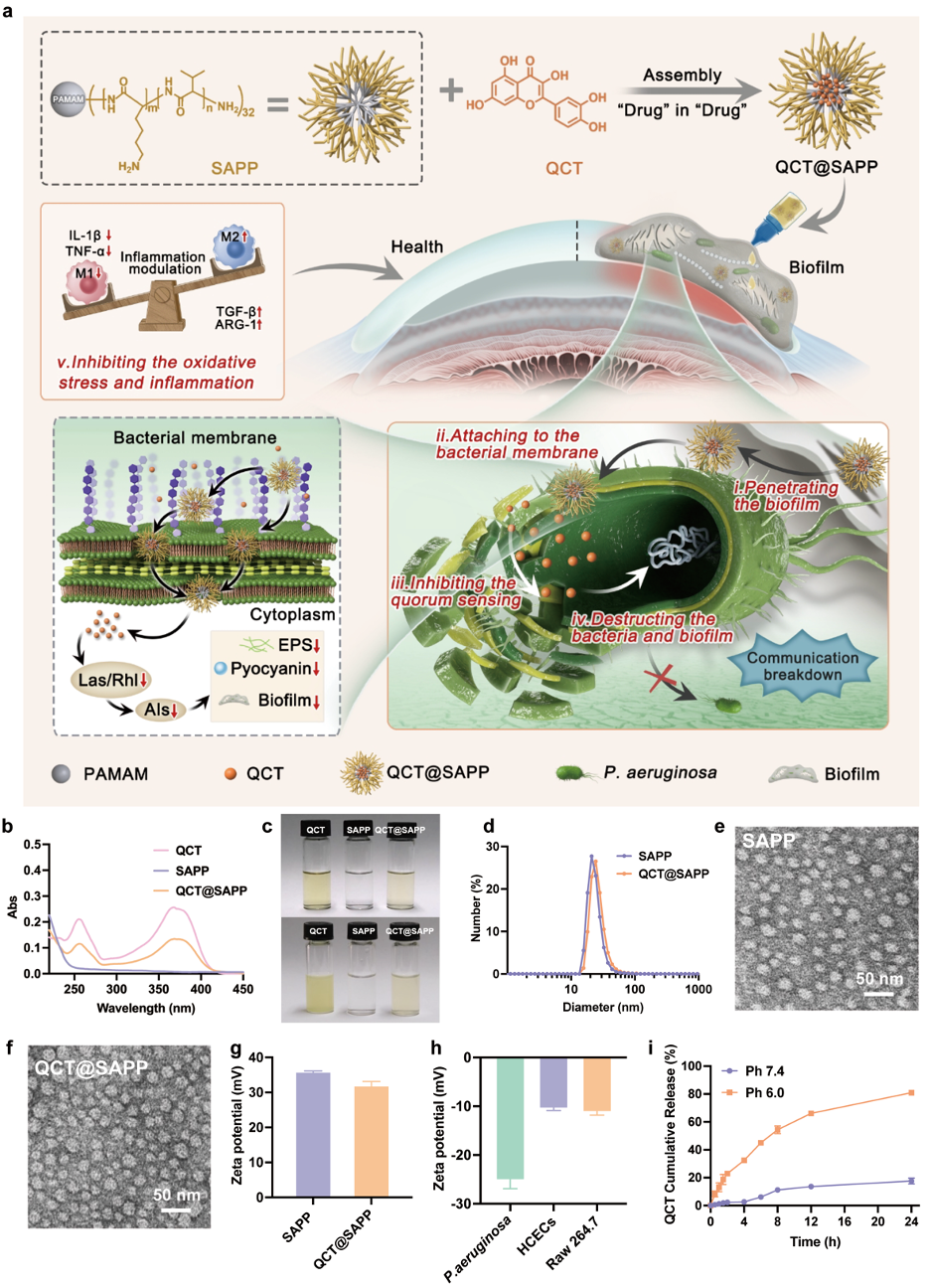
图1. 抗菌复合物QCT@SAPP的制备与作用示意图
细菌性角膜炎是一种发展迅速的眼部感染,通常由细菌侵袭角膜引起,伴随严重的炎症反应和眼表损伤,严重威胁视力健康。尤其是由铜绿假单胞菌(P. aeruginosa)引起的角膜炎,其侵袭性极强,往往在短短几天内对整个角膜造成毁灭性破坏。若未能及时治疗,可能引发角膜溃疡、穿孔甚至导致失明。然而,现有的以抗生素类眼药水为主的治疗手段,在面对复杂的细菌生物被膜时效果受限。细菌通过在眼表形成生物被膜,借助其复杂的结构和微环境,能有效抵御抗生素的攻击。尤其是当细菌突变时,常规抗菌药物的效果会大打折扣。为此,亟需寻找一种能够有效突破生物被膜屏障杀灭细菌的创新疗法。
QCT@SAPP的成功研发,为治疗难治性细菌性角膜炎提供了新的希望。通过其独特的群体感应抑制机制和生物被膜破坏能力,QCT@SAPP有望成为未来眼科领域的一种创新疗法,极大提升细菌性角膜炎的治疗效果,同时降低耐药性风险,助力患者恢复视觉健康。这项研究不仅为眼科治疗带来新的突破,也为抗生物被膜治疗领域提供了宝贵的经验,未来可能在更多细菌感染治疗中得到应用。
原文链接:https://doi.org/10.1021/acsnano.4c12195
2
干眼症是一种以泪膜稳态破坏为特征的多因素疾病,虽然主要与年龄相关,但频繁使用屏幕和佩戴隐形眼镜导致年轻人患病率增加。刺激、灼烧、轻度至重度眼部炎症、眼痒疲劳都是干眼的特征。眼部炎症和泪膜高渗成为干眼症的标志。另外,泪膜的高渗透压可以触发氧化应激途径,在干眼症患者泪膜和眼表中观察到氧化应激水平升高,与眼表功能的各种临床指标相关。铁死亡,其特征是铁依赖性脂质过氧化和活性氧(ROS)水平升高。最近,在干眼症的进展中观察到铁死亡,提示通过靶向铁死亡是干预干眼症的一种潜在方式。
近日,浙江大学医学院附属第二医院眼科中心/浙江大学眼科医院姚克教授和韩海杰研究员团队以铁死亡这一非凋亡程序性细胞死亡方式为切入点,开发了一种抗铁死亡和抗炎协同作用的新型角膜粘蛋白靶向修饰的脂质体滴眼液,在体内外均可破坏炎症级联、ROS生成和铁死亡,为有效缓解干眼症状提供了一个有效的解决方案。该研究以“Corneal Mucin-Targeting Liposome Nanoplatforms Enable Effective Treatment of Dry Eye Diseases by Integrated Regulation of Ferroptosis and Inflammation”为题发表在《ADVANCED SCIENCE》上(Adv. Sci., 2025, 12(3):2411172)。浙二眼科中心实验室技术员张尹、硕士研究生周婷莲和王凯医生为论文共同第一作者。该研究得到了国家自然科学基金,浙江省自然科学基金,浙江省重点研发项目和中国博士后科学基金资助。

这种负载环孢素A(CsA)和铁死亡抑制剂(Fer-1)的唾液酸靶向肽修饰的脂质体(CF@SNPs)通过抑制ROS生成,p53- SLC7A11-GSH依赖性铁死亡和TNF-α相关的炎症级联反应来减轻干眼症状。同时,CF@SNPs具有良好的生物安全性和眼耐受性,为有效缓解干眼症状提供了一个有希望的解决方案,在治疗干眼症中具有未来临床应用的潜力。
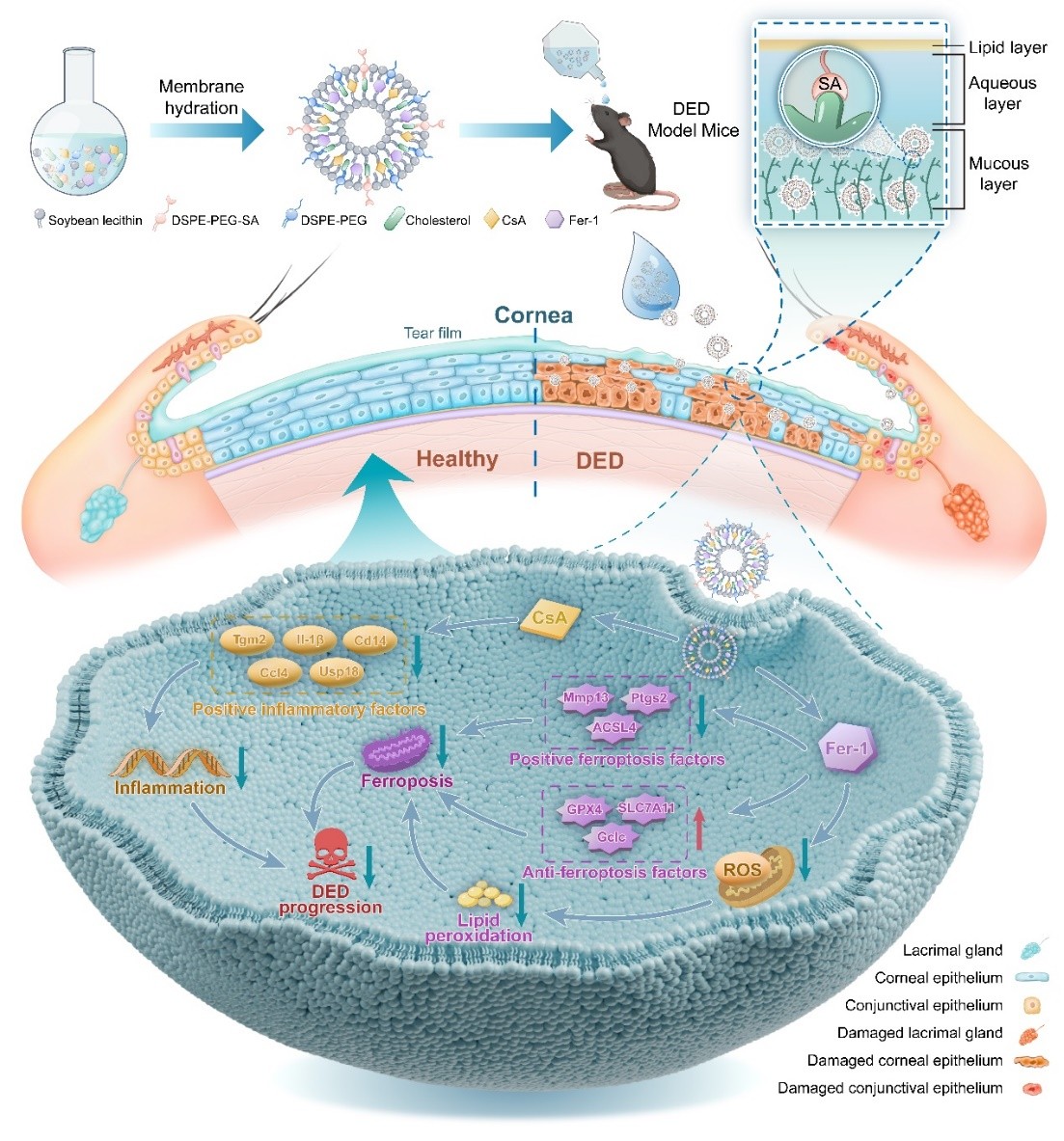
图2. CF@SNPs治疗干眼的疗效及机制示意图
原文链接:https://doi.org/10.1002/advs.202411172
3
浙江大学医学院附属第二医院眼科中心/浙江大学眼科医院姚克教授和韩海杰研究员团队以角膜损伤修复过程中,“基底膜受损导致角膜上皮来源细胞因子放大损伤愈合级联反应,导致瘢痕形成”这一病理机制为切入点,突破主流研究致力于促进损伤愈合而忽略瘢痕形成的局限性,创新性地结合组织工程学手段,提出通过重建基底膜屏障来调控损伤愈合级联反应,实现角膜有序再生和修复的新策略。该基底膜仿生水凝胶既能用于预防角膜损伤后瘢痕形成,又能替代角膜移植术去除已有的角膜瘢痕,实现“防治一体”。该研究以“Biologically inspired bioactive hydrogels for scarless corneal repair”为题发表在《Science Advances》上(Sci. Adv., 2024,10(51):eadt1643)。文章第一作者是浙江大学博士研究生黄佳男、蒋拓颖和郄继巧。该研究得到国家自然科学基金委和浙江省重点研发计划的支持。
角膜盲是仅次于白内障的第二大致盲性眼病,全球范围内有1200多万角膜盲患者。角膜外伤、感染等多种疾病均会对角膜的正常结构和生理机能造成破坏,引发角膜损伤愈合级联反应,导致角膜瘢痕性失明。角膜上皮基底膜是在角膜上皮和基质层之间形成的高度特化的细胞外基质。其功能在于锚定角膜上皮细胞,支持其生长分化;并且可以通过结合局部细胞因子,调节其浓度,从而影响细胞功能。在角膜损伤的背景下,上皮基底膜屏障被破坏,使得上皮来源的细胞因子大量涌入基质层,放大损伤愈合级联反应,造成角膜瘢痕。由此可见,基底膜屏障对于决定角膜损伤愈合的结局具有关键作用。
本研究构建了基底膜仿生水凝胶,用于角膜损伤的治疗。该研究从剖析人角膜基底膜的组分入手,通过透射电镜、免疫染色等手段,确定了基底膜的重要组分,包括胶原和硫酸肝素。进一步借助模拟计算分析,验证肝素对于角膜损伤相关细胞因子具有良好的吸附作用。基于前期结果,研究人员将胶原蛋白衍生的明胶和高度硫酸化的肝素经修饰后,制备得到了基底膜仿生水凝胶。仿生水凝胶具有良好的吸附角膜损伤相关细胞因子的能力,并限制因子的扩散,从而模拟了天然角膜基底膜的屏障功能。在新西兰兔和食蟹猴角膜损伤模型中,基底膜仿生水凝胶均有效促进了角膜损伤愈合,并显著抑制了角膜纤维化的进展(图3)。
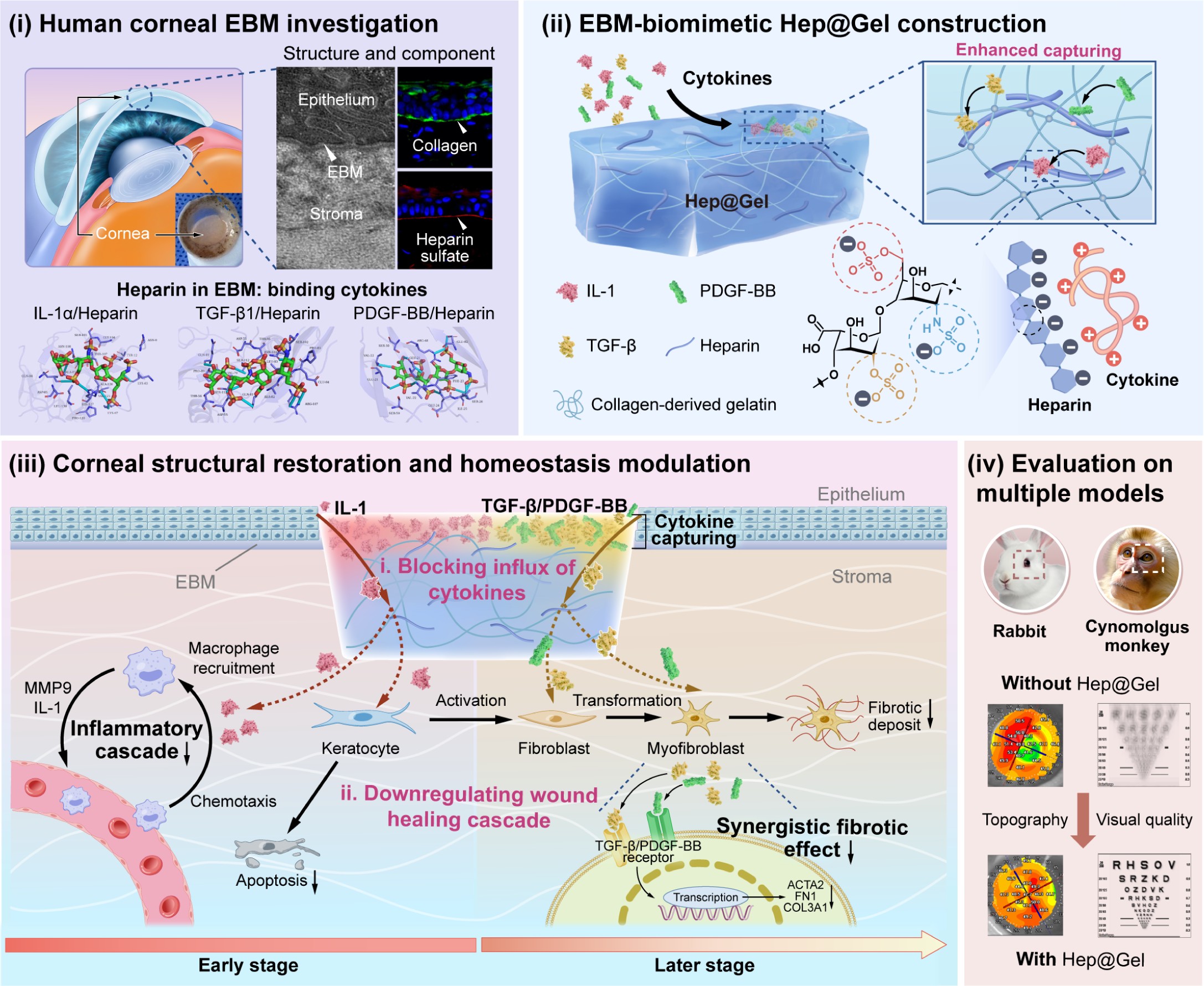
图3. 基底膜仿生水凝胶促进角膜损伤少瘢痕化愈合
原文链接:https://www.science.org/doi/10.1126/sciadv.adt1643